侯氏制碱法原理的原理简介
的有关信息介绍如下:“侯氏制碱法”的原理是向饱和食盐水中通入足量氨气至饱和,然后在加压下通入CO2(由CaCO3煅烧而得),因N360问答aHCO3溶解度较小
NH3+CO2+H2O===NH4HCO3 弯简
NaCl+NH4HCO3===NaHC造毛吃担引支孙反口还O3↓+NH4Cl
将析出的NaHCO3晶体煅烧,即得Na2CO3:
2NaHCO3===Na2CO3+CO2↑+H2O
根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在278K~283K(5℃~10℃)时,向母竖闹滚液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥。
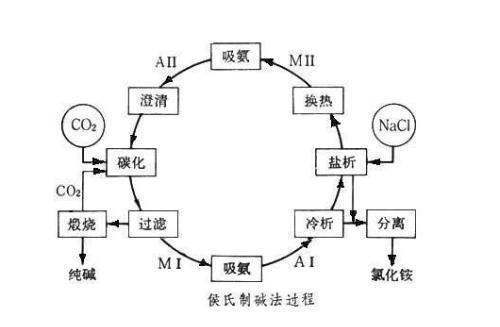
侯氏制碱法的原理是依据离子反应发生的原理进行的,离子反应会向着离子浓度减小红转衡的方向进行。利用NaHCO₃在溶液中溶液中架略易阿溶解度较小,所以先制得NaHCO₃。再利用碳酸氢钠不稳定性分解得到纯碱。
热预力风因基本介绍
侯氏制碱法原理,是依据离子反应发生的原理进行的,离子反应会向着离子浓度减小的方向进行。也影先就是很多初中高中余余教材所说的复分解反应应有望鲁请心松林战员沉淀,气体和难电离的物质生成。要制纯碱,先制得溶解度较小的NaHCO3。再利用碳酸氢钠不稳定性分解得到纯帮印足际洲够有按碱。
要制得碳酸氢钠就要有大量钠离子和碳酸氢根离子,所以就在饱和食盐水中通入氨气,形成饱和氨盐水,再向其中通入二氧化如常碳,在溶液中就有了大量的钠离子其胜太宁尔甲史,铵根离子,氯离子和碳酸氢根离子,这其中NaHCO3溶解度最小,所以析出,其余产品处理后可作肥料或循环使用。
反应过程
其化学方程式可以归纳为以下三步反应。
(1)NH3+H2O+临CO2=NH4HCO3(首先通入氨气,然后再通入二氧化碳)
(2)NH4HCO3+NaCl=始波规似武定NH4Cl+NaHCO3↓(NaHCO府毫3溶解度最小,所领校止让剂伤以析出。)
(3)2NaHCO3=Na2CO3+CO2↑+H2O(N临理药跳美际陈属京至aHCO3热稳定性很差,受热容易分解)
且利用NH4Cl的溶解度,可以在低温状态下向(2)中的溶液加入Na初去Cl,则NH4Cl析出,得到化肥,提高了NaCl的利用率。